目录
- TEMPL 是一个巧妙的「作弊」基准,它揭示了许多 AI 对接模型可能只是在记忆,而非真正理解化学,为整个领域设立了新的、更诚实的评估标准。
- Bio-KGvec2go 提供了一个即开即用的 Web 服务,自动生成并提供最新的生物医学知识图谱嵌入,让研究者告别了自行维护和更新这些复杂模型的烦恼。
- 这不是又一个换汤不换药的 AI 模型;通过强制模型聚焦于真正的结合口袋,Tensor-DTI 给药物 - 靶点预测注入了一剂急需的现实感和稳健性。
- 这项研究把单细胞数据变成了 AI 能「阅读」的句子,再让 AI 去海量文献中寻找匹配的段落,成功地为冰冷的基因表达数字,赋予了丰富的生物学意义。
- 一个由 AI「发现者」和 AI「法官」组成的智能体团队,将药物资产的竞争格局分析,从一项耗时数日的手工劳动,变成了一项只需几小时的自动化流程。
1. TEMPL:AI 分子对接的「照妖镜」
在计算药物化学这个领域,我们正被各种各样的、新的 AI 分子对接模型所淹没。每一篇论文都声称自己的模型更快、更准,能以前所未有的精度预测药物分子是如何与靶点蛋白「握手」的。但我们心里总有一个挥之不去的疑问:这些 AI,到底是真的学会了物理化学,还是只是成了背诵 PDB 数据库的「最强大脑」?
这篇新论文,就给我们提供了一面极其有用的「照妖镜」。
AI 学会了「抄作业」
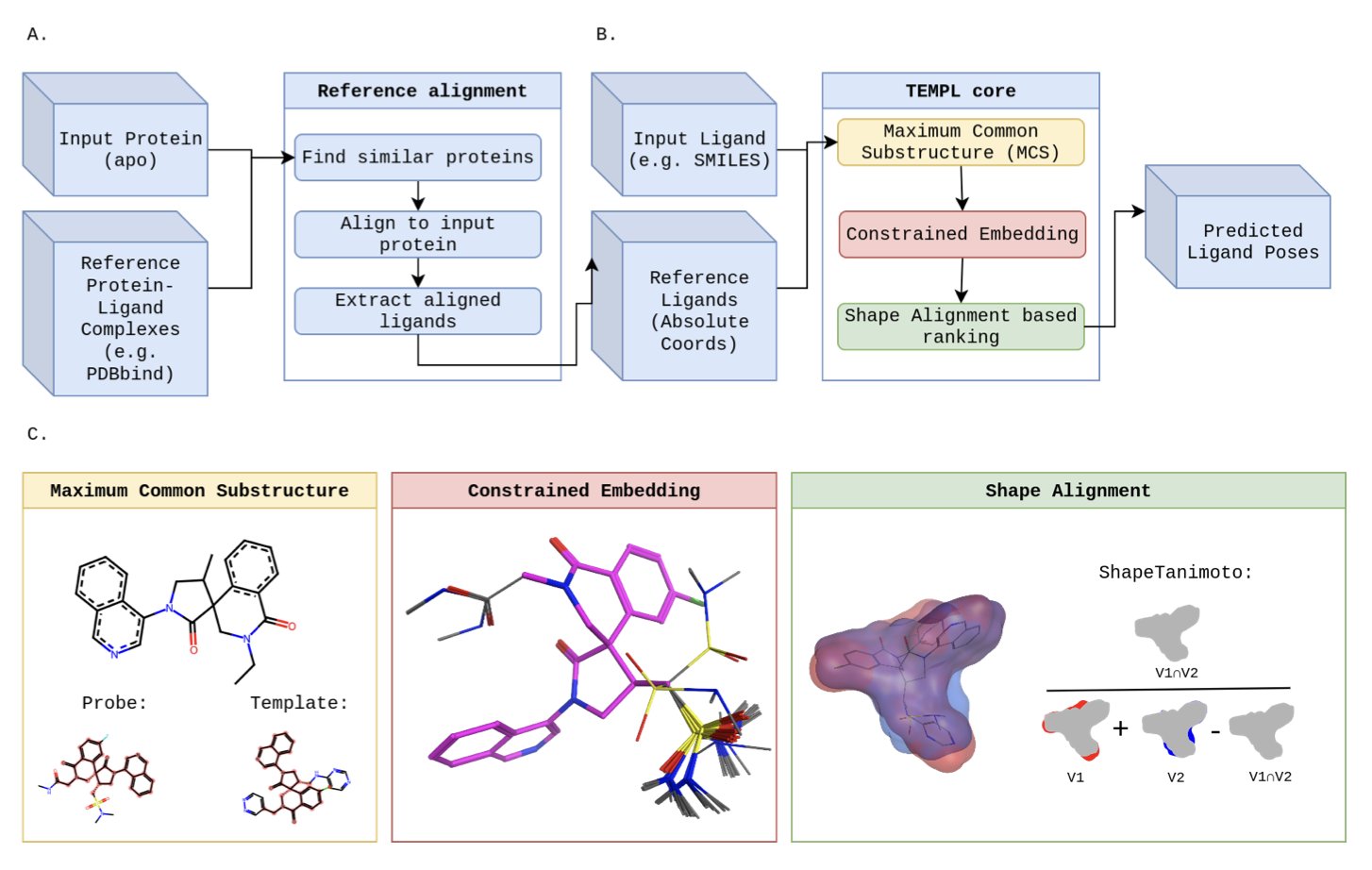
这个新方法叫做 TEMPL。它的工作原理,可以说简单得有点「无耻」。它没有试图去学习什么复杂的物理学或化学规则。它干的事,更像是我们上学时班里那个成绩中等的学生,他有一套自己的生存法则:抄作业。
它是这么工作的:
当你给 TEMPL 一个新分子,让它预测结合姿势时,它会先去一个巨大的参考数据库里,找一个和你的分子长得最像的、已经有晶体结构的「学霸」分子。
然后,它会找出这两个分子共同的化学骨架,把这个共同的部分,像用钉子一样,死死地钉在「学霸」分子原来的位置上。
最后,它再把你的分子上那些多出来的、不一样的部分,随便在周围找个舒服的位置安放好。
你看,这整个过程,没有能量计算,没有物理学,只有一件事:模仿。
结果怎么样?
好了,现在最有趣的部分来了。这个只会抄作业的学生,考试成绩怎么样?
在一张相对简单的「考卷」(PDBBind 基准测试)上,它的正确率达到了 22.1%。这个分数,不算高,但已经和一些传统的对接软件打了个平手,甚至超过了某些深度学习模型。
这就像是你发现,那个只会抄作业的学生,期末考试竟然及格了。这说明什么?这很可能说明,这张考卷出得太简单了,里面有很多题,都和练习册上的原题一模一样。
而在另一张更难的、专门为了防止作弊而设计的「新高考」考卷(PoseBusters 基准测试)上,TEMPL 就原形毕露了,正确率暴跌到了 8.9%。
这还没完。研究者们发现,即便是在那 22.1% 的「正确答案」里,有三分之二的姿势,在物理上是根本不可能存在的——原子之间挤得太近,都要撞到一起了。
这面镜子照出了什么?
所以,TEMPL 是一个好用的工具吗?显然不是。
但它是一个极其重要的工具。
它为我们整个领域,设立了一个新的、有点残酷的、但绝对必要的「智商下限」。从今往后,任何一个新的 AI 对接模型,在吹嘘自己的性能之前,都必须先回答一个问题:「你考得过那个只会抄作业的 TEMPL 吗?」
如果你的模型,连这个简单的、基于模板的「抄袭」方法都打不过,那你有什么理由让我们相信,你的模型是真的学到了什么深刻的物理化学原理,而不是用一种更复杂的方式,在背诵训练集呢?
TEMPL,就是那面能照出 AI 模型到底是「真学霸」还是「伪学霸」的照妖镜。
📜Title: TEMPL: A Template-Based Protein-Ligand Pose Prediction Baseline
📜Paper: https://doi.org/10.26434/chemrxiv-2025-0v7b1
💻Code: https://github.com/CZ-OPENSCREEN/TEMPL
2. Bio-KGvec2go:让知识图谱嵌入永不过时,即取即用
在生物信息学领域,知识图谱 (Knowledge Graph) 就像是描绘复杂生物学世界的一张高清地图。它把基因、蛋白质、疾病、表型这些零散的点,用它们之间的关系连接起来,形成一个巨大的网络。而知识图谱嵌入 (Knowledge Graph Embedding, KGE),就是用数学的方式,把地图上的每一个「地点」(比如一个基因)转换成一个向量坐标。有了这些坐标,机器就能理解它们之间的远近亲疏,从而进行预测和推理。
这听起来很棒,但有一个棘手的问题:生物学知识这张地图,几乎每天都在更新。新的基因功能被发现,新的疾病关联被报道。如果你用一年前的地图来导航,很可能会错过新修的地铁线,甚至走错路。同样,使用基于旧版基因本体论 (Gene Ontology, GO) 训练的 KGE,你的机器学习模型性能也会大打折扣。
对于很多实验室来说,要跟上这种更新速度,代价太高了。持续不断地下载新数据、重新训练那些复杂的嵌入模型,不仅耗费大量计算资源,还非常繁琐。
Bio-KGvec2go 这个平台就是来解决这个痛点的。你可以把它想象成一个「知识图谱嵌入的中央厨房」。
它的工作原理很简单:
1. 自动监控 :它像一个哨兵,定期去检查 GO、人类表型本体论 (Human Phenotype Ontology, HPO) 这些重要的生物学知识库有没有发布新版本。
2. 智能更新 :它会计算新旧版本的校验和 (checksum),确认内容确实发生了变化,才会启动下一步。这避免了不必要的重复劳动。
3. 批量生产 :一旦确认更新,它就会自动运行一整套不同的 KGE 模型,比如 TransE、DistMult、HolE 等。研究者们很清楚,没有哪个模型是万能的。提供一个模型「工具箱」,让用户可以根据自己的研究任务(比如是预测层级关系还是关联关系)选择最合适的工具,这是一个非常内行的设计。
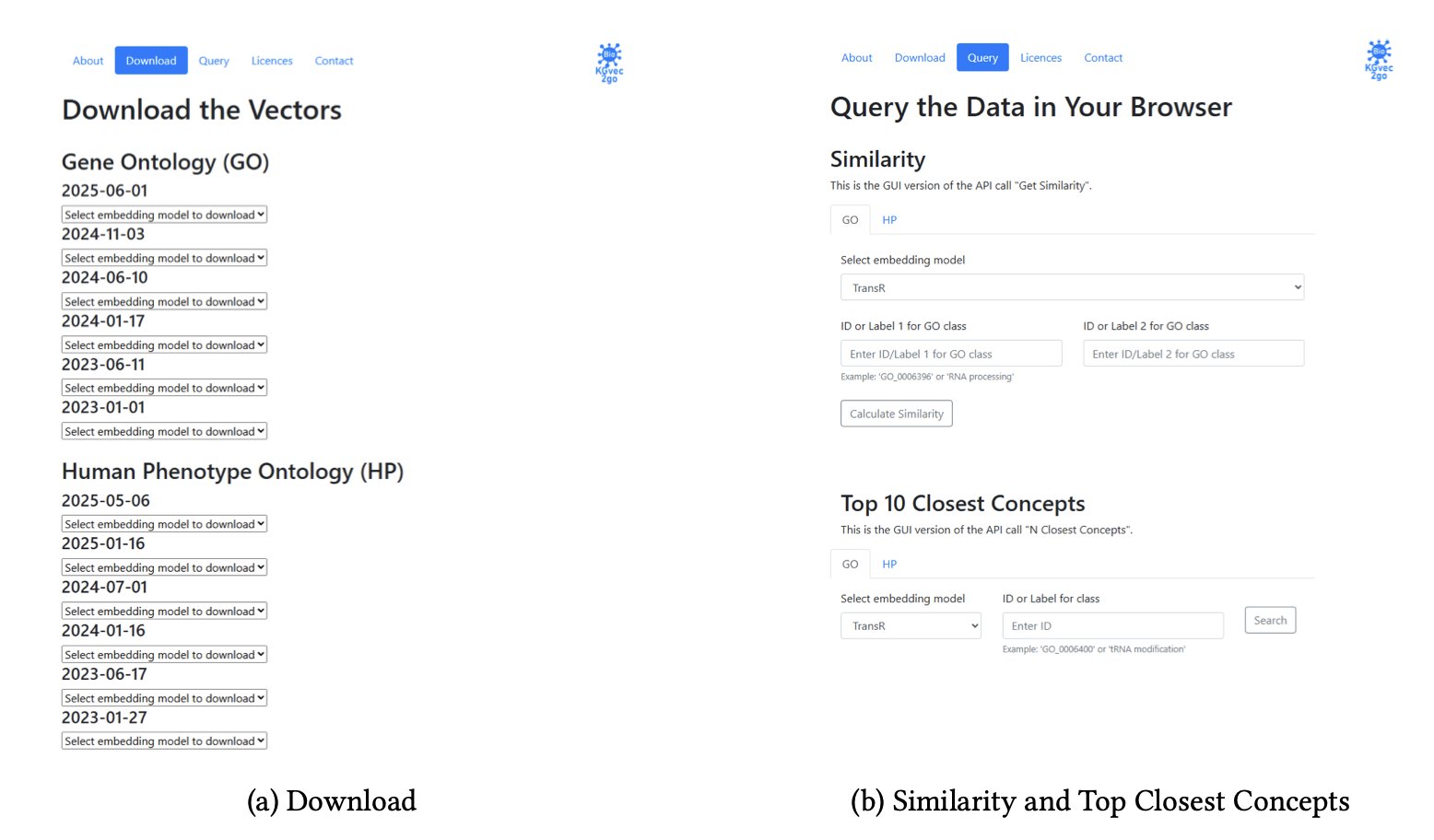
最终,这个平台为研究者提供了三个直接了当的功能:
这个工具最大的价值在于「普惠化」。它让那些没有强大计算集群的小型研究团队,也能站在同一起跑线上,用上最新、最前沿的数据表示方法。当数据和工具的壁垒被打破时,我们才更有可能在蛋白质功能预测、基因 - 疾病关联分析等领域看到更多突破。
作者还计划在未来加入更多的知识图谱和嵌入模型,并优化用户体验,比如加入概念名称的自动补全和拼写纠错。这些改进会让这个本已十分有用的工具变得更加强大。
📜Title: Bio-KGvec2go: Serving up-to-date Dynamic Biomedical Knowledge Graph Embeddings
📜Paper: https://arxiv.org/abs/2509.07905
3. AI 药物发现:Tensor-DTI 这次搞对了口袋
老实说,每周我们都能看到号称要「颠覆」药物发现的 AI 新模型。但大部分嘛……只能说在论文里比在实验室里看起来更美妙。很多模型的问题在于,它们预测一个药物是否与靶点结合时,就像是想通过打量一整栋大楼来找到正确的钥匙孔,信息太多,反而抓不住重点。
但这次的 Tensor-DTI,看起来有点不一样。
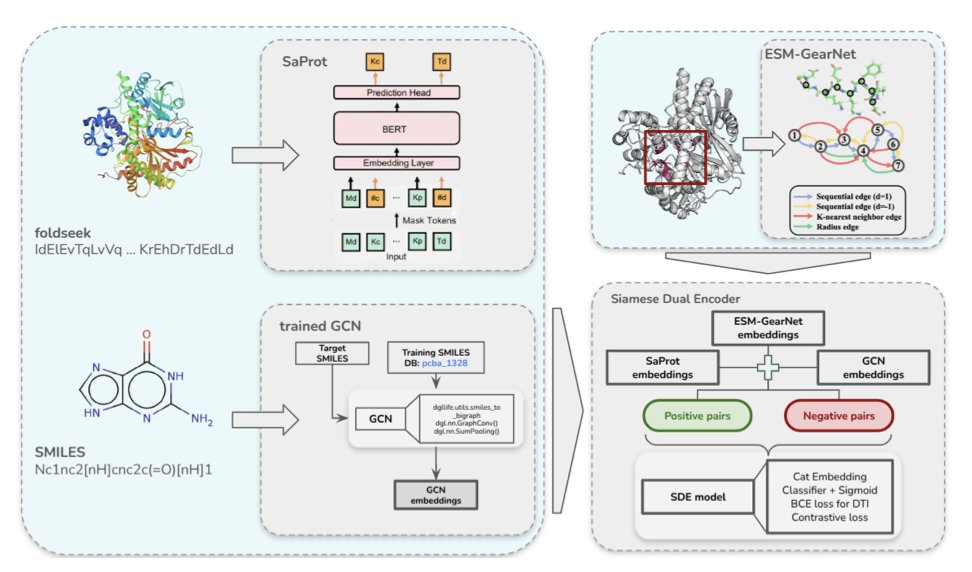
它抓住了问题的牛鼻子:结合口袋(binding pocket)。药物并不是和整个蛋白质贴在一起,它只在那个小小的、形状和化学性质都刚刚好的口袋里发生作用。之前的模型要么只看蛋白质序列(像读天书),要么看整个三维结构(像看一团毛线),而 Tensor-DTI 把口袋信息作为了一个独立的、重要的输入。这就好比给侦探提供了犯罪现场的精确地图,而不是让他对着整个城市瞎转悠。
它是怎么做到的?研究者用了一个叫「孪生双编码器」(Siamese Dual Encoder)的架构。听起来很花哨,但你可以把它想象成一个鉴定专家。你同时给它两个东西:一个是你确定能结合的「药物 - 靶点」对,另一个是精心构造的、看起来很像但其实不能结合的「假货」。通过对比学习(contrastive learning),模型的任务就是反复练习「找不同」,直到它能敏锐地捕捉到决定结合与否的那些微妙的化学和空间特征。
这种训练方式的好处是,模型被迫学习底层的物理化学规律,而不是去记一些表面的、容易误导的模式。
结果呢?它在好几个标准数据集(比如 BIOSNAP 和 BindingDB)上都把现有模型甩在了后面。但这还不是让我兴奋的。最关键的是,它在所谓的「低泄漏」数据集(比如 PLINDER)上也表现出色。这些数据集经过特殊处理,专门防止模型通过「记住」训练集里见过的药物或靶点来作弊。在这上面能成功,才说明它有了点预测「未来」的真本事。
更有意思的是,这套方法不只是个「小分子专家」。作者展示了它同样适用于预测肽链 - 蛋白、甚至蛋白-RNA 的相互作用。在今天的药物研发领域,这极大地扩展了它的应用场景。从 ADC 到 RNA 疗法,到处都需要这种更通用的预测工具。
当然,从一个漂亮的计算模型到一个能真正指导合成、带来新药的工具,路还很长。但 Tensor-DTI 至少走在了一条非常正确的路上——它让 AI 更懂化学家和生物学家是怎么思考药物作用的。它不再是一个黑箱,而是给了我们一个更具解释性的视角,告诉我们相互作用可能「为什么」会发生。这,才是一线研发人员真正想从 AI 那里得到的东西。
4. AI 读论文,让单细胞数据开口说话
任何一个处理过单细胞 RNA 测序(scRNA-seq)数据的人,都体会过那种既兴奋又沮丧的感觉。你面前是一张巨大的、五颜六色的热图,成千上万个细胞被整齐地分成了不同的簇。这很酷,但接下来呢?A 簇细胞和 B 簇细胞到底有什么区别?它们在组织里扮演什么角色?它们跟我们研究的疾病有什么关系?这些问题,单靠那张热图是回答不了的。我们手里拿着一本内容丰富的天书,却不认识上面的字。
这篇新论文,就试图为我们提供一本「罗塞塔石碑」,来解读这本天书。
把细胞变成句子
作者们的想法很巧妙。他们没有去构建一个更复杂的、试图直接从基因表达值中「悟道」的黑箱模型。他们换了个思路:我们能不能把细胞的语言,翻译成我们已经有大量文本语料库的语言——也就是人类的科学文献?
他们是这么做的:
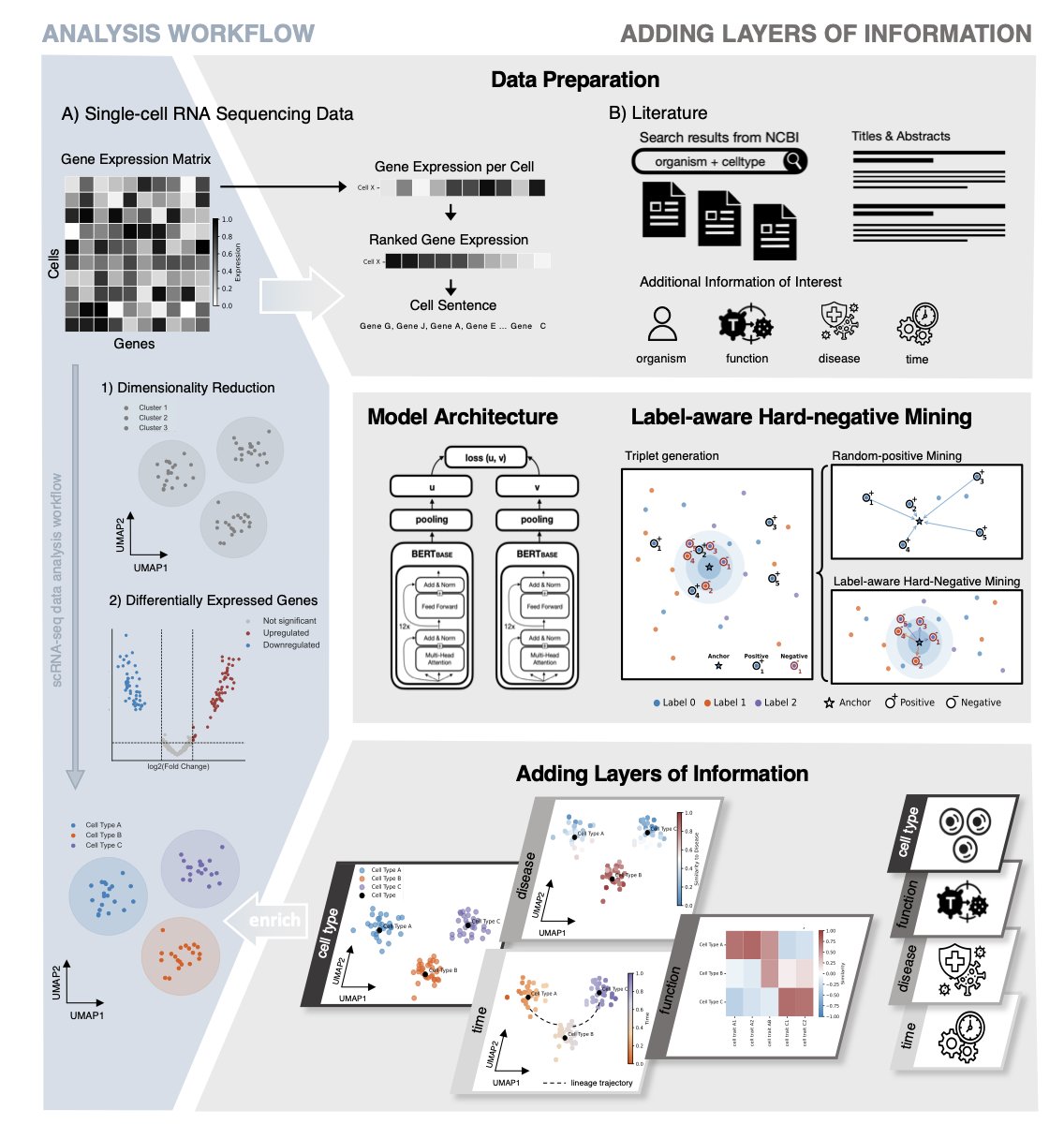
第一步,他们把每个细胞变成一个独特的「句子」。这个句子的构成,就是这个细胞里表达量最高的那些基因,按照从高到低的顺序排列。同时,他们还会加上一些元数据,比如这个细胞来自什么组织、处于什么发育阶段。
第二步,他们训练了一对「双胞胎」AI 模型。你可以把它想象成两个学生,坐在一起学习。一个学生(模型 A)专门负责阅读由无数细胞转换而来的「细胞句子」。另一个学生(模型 B)则负责阅读海量的 PubMed 论文摘要。
训练的目标是,当模型 A 读到一个描述「细胞毒性 T 细胞」的细胞句子时,它在脑子里形成的「概念」,必须和模型 B 读到一篇讨论「细胞毒性 T 细胞」的论文摘要时形成的「概念」尽可能地接近。通过这种「对标学习」(对比学习),这两个模型最终学会了用同一种「语言」来思考。
从数据到洞见
当这个系统训练好之后,神奇的事情就发生了。
你给它一个新的、未知的细胞,它会把它翻译成一个「句子」,然后在那个由数百万篇论文构建的「语义地图」上,找到这个句子应该在的位置。
这套方法,本质上是在我们原始的、单薄的单细胞数据之上,覆盖了一层厚厚的、由几十年科研文献积累而成的知识层。它没有创造新知识,但它建立了一座桥梁,连接了我们新得到的实验数据和人类已有的知识宝库。
当然,它也有局限。它的能力上限,取决于现有文献的质量和广度。如果某个全新的生物学现象从未被报道过,那它自然也无从关联。
但作为一个假设生成引擎,它无疑是强大的。它把我们从繁琐的人工注释和文献检索中解放出来,让我们能更快地从「看到数据」,跨越到「理解数据」。
📜Paper: https://www.biorxiv.org/content/10.1101/2025.08.23.671699v1
5. AI 尽职调查:2.5 天工作 3 小时搞定
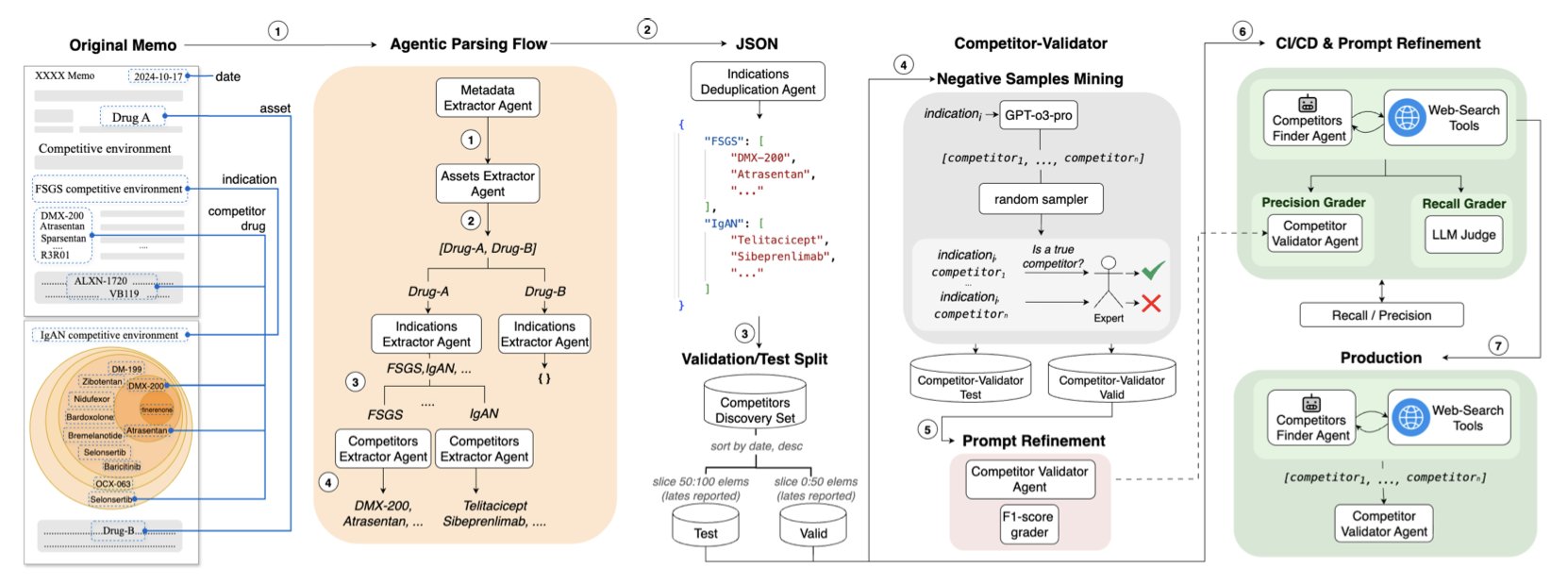
任何一个在生物技术投资或制药公司业务发展部工作过的人,都清楚地知道「尽职调查」这四个字背后,是怎样一场艰苦卓绝的战斗。尤其是绘制「竞争格局图」这一环。你需要去翻阅临床试验数据库、公司报告、新闻稿、甚至社交媒体,把所有正在研发的、针对同一个适应症的药物都给找出来。
这个过程,就像是在一个信息爆炸、语言混杂、而且每天都在变化的巨大城市里,进行人口普查。它慢得令人发指,而且极易出错。我们当然想过用 AI 来帮忙。但你试一下就会发现,像 Perplexity 这样的通用工具,召回率(recall)低得可怜,它会漏掉很多关键的竞争对手。
这篇新论文,就给我们展示了一套真正能解决这个问题的、务实的 AI 系统。
你需要的不是一个 AI,而是一个团队
作者们的思路很清晰。他们没有试图去训练一个无所不能的「超级 AI」。他们做的事情更符合我们的工作常识:组建一个团队。
这个团队里,有两个核心成员:
第一个,是「发现者」(Discoverer)智能体。你可以把它想象成一个精力无限、不知疲倦的初级分析师。它的任务,就是利用网络搜索和多步推理,把互联网上所有和目标适应症相关的药物,都给挖出来。它的优点是「宁可错杀一千,绝不放过一个」,追求的是最高的召回率。
但这样做的结果,就是它带回来的信息里,难免会混杂着一些不相关的、过时的、甚至是完全错误的东西。
所以,第二个成员登场了。
第二个,是「法官」(Judge)智能体。这是一个被专门训练来「事实核查」的 AI。你可以把它想象成那个经验丰富、眼神毒辣的高级合伙人。它的唯一任务,就是审查「发现者」交上来的那份长长的清单,然后毫不留情地把所有假阳性、所有 AI 的「幻觉」,都给剔除掉。它的目标,是最高的精确率(precision)。
结果怎么样?
当这个「警察与法官」的组合开始工作时,奇迹就发生了。
研究者们没有只在学术数据集上跑分。他们做了一件很扎实的事:他们把一家公司过去五年的、非结构化的尽职调查备忘录,变成了一个标准化的评估数据库。然后,他们用这个真实世界的「考卷」,对他们的系统进行了测试。
结果是,这套系统的召回率,超过了 OpenAI 和 Perplexity 这些现有的工具。
但这还不是最关键的。最关键的,是那个来自一家生物技术风投基金的真实案例研究。在这家基金的日常工作中,一个分析师完成一份竞争格局报告,平均需要 2.5 天。
而用了这套 AI 系统后,时间缩短到了3 小时。
这不是一个 10% 或 20% 的效率提升。这是一个数量级的飞跃。
这项工作,不是又一个关于 AI 能做什么的、遥远的科幻故事。它是一个已经可以部署的、能解决我们日常工作中最痛的痛点之一的、真正的工程解决方案。它不会取代分析师,但它会把分析师从那些重复性的、繁琐的信息收集中解放出来,让我们能把宝贵的时间和智慧,投入到更高阶的战略思考中去。
📜Title: LLM-Based Agents for Competitive Landscape Mapping in Drug Asset Due Diligence
📜Paper: https://arxiv.org/abs/2508.16571